
2022年11月29日,国际知名杂志《Biomaterials》报道了北航生物与医学工程学院、北京市生物医学工程高精尖创新中心李晓光教授团队在脊髓损伤修复后新生神经元的正确连接控制膀胱功能方面取得新进展:《Proper wiring of newborn neurons to control bladder function after complete spinal cord injury》。脊髓损伤修复领域长期致力于如何促进受损的轴突实现长距离轴突再生。李晓光教授团队的前期研究提出了一种新的修复理论:通过诱导内源性神经发生建立新的中继神经环路,桥接受损的头尾两端以恢复受损的神经功能。然而,这些新生的中继神经环路是否可正确整合到受损的长投射神经环路中及其整合机制目前是未知的。李晓光教授团队首次阐明,应用活性生物材料诱导内源性新生神经元产生,并促进其正确整合到受损的长投射排尿神经环路中。即使脑桥Barrington’s 核到腰骶段脊髓的长投射神经轴突没有再生,但新生的中继神经元可正确桥接控制排尿的脑高级中枢和脊髓低级中枢,重建排尿反射神经环路,并有效恢复脊髓损伤后的膀胱功能。该研究不仅首次揭示了新生中继神经环路在脊髓损伤后功能恢复中的重要作用,也为脊髓损伤后神经源性膀胱功能障碍提供一种新的对因治疗策略。
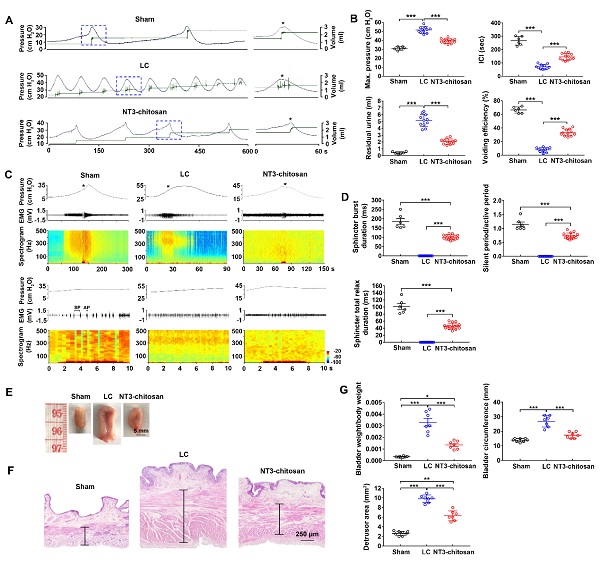
图1. NT3-壳聚糖改善脊髓损伤大鼠神经源性下尿路功能障碍(A-D),减少膀胱组织重塑(E-G)。
脊髓损伤不仅可引起损伤平面以下感觉和运动功能障碍,而且可引起严重的膀胱功能障碍,导致尿潴留、尿频、尿急和尿失禁,长期可引起严重的尿路感染、结石甚至终末期肾病,是脊髓损伤病人常见的死亡原因之一。神经源性膀胱功能障碍的理想治疗是重建排尿反射神经环路,使膀胱重获脊髓上高级脑中枢的控制,进而恢复有效性自主性排尿。这可明显改善脊髓损伤病人的生活质量,增加社会参与度,减少并发症,降低死亡率。李晓光教授团队采用天然生物材料-壳聚糖复合神经营养因子(NTs)构建了系列新型活性生物材料,可长期缓释神经营养因子达14周,通过改善损伤区局部微环境,激活内源性神经干细胞,募集其迁移到损伤区分化为功能成熟的神经元,并与宿主细胞形成功能性的神经网络,最终促进功能恢复。研究成果于2015年至2022年发表在《STTT》、《PNAS》、《Progress in Neurobiology》、《Biomaterials》等一系列国际著名期刊上。
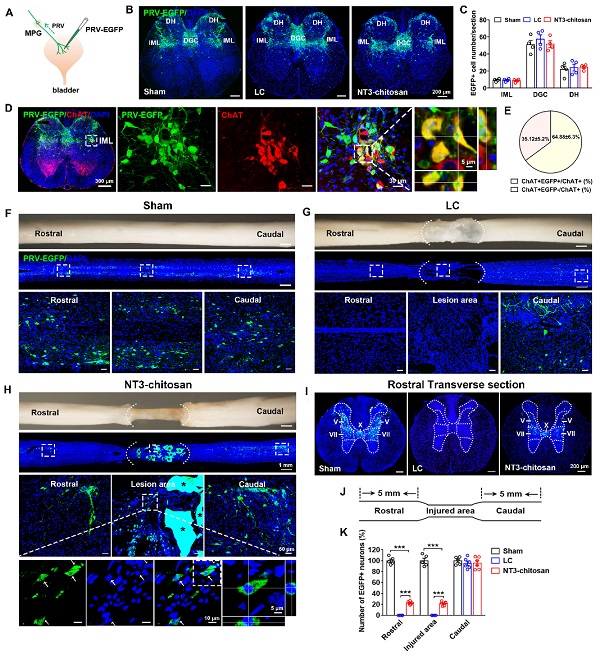
图2. 逆行跨多突触病毒示踪显示NT3-壳聚糖重建脊髓损伤后排尿反射神经环路。
本论文在胸段完全横断性脊髓损伤区植入NT3-壳聚糖生物活性材料,应用尿流动力学和肌电图等方法证明其可明显减少脊髓损伤大鼠膀胱过度活动,改善膀胱逼尿肌和尿道外括约肌的协同性,有效恢复膀胱功能。应用逆行跨多突触病毒(PRV)示踪结果显示,将PRV注射到大鼠膀胱壁后,可在修复组大鼠脊髓损伤区、损伤区头端脊髓以及控制排尿的脑高级中枢检测到PRV阳性细胞。应用多重免疫荧光染色技术发现,在脊髓损伤区,这些PRV阳性细胞是BrdU/NeuN双阳性的,且既有兴奋性中间神经元,也有抑制性中间神经元,提示这些新生神经元可正确整合到排尿反射神经环路中。应用逆行跨单突触病毒示踪和顺行病毒示踪证明,新生的中继神经元可正确桥接控制膀胱的脊髓低级中枢和脊髓上脑高级中枢,即使在没有明显的长距离轴突再生的情况下。应用光遗传学和化学遗传学等方法证明,NT3-壳聚糖可重新恢复脊髓损伤大鼠下尿路的脊髓上控制,同时强调了新生神经元在膀胱功能恢复中的重要作用。
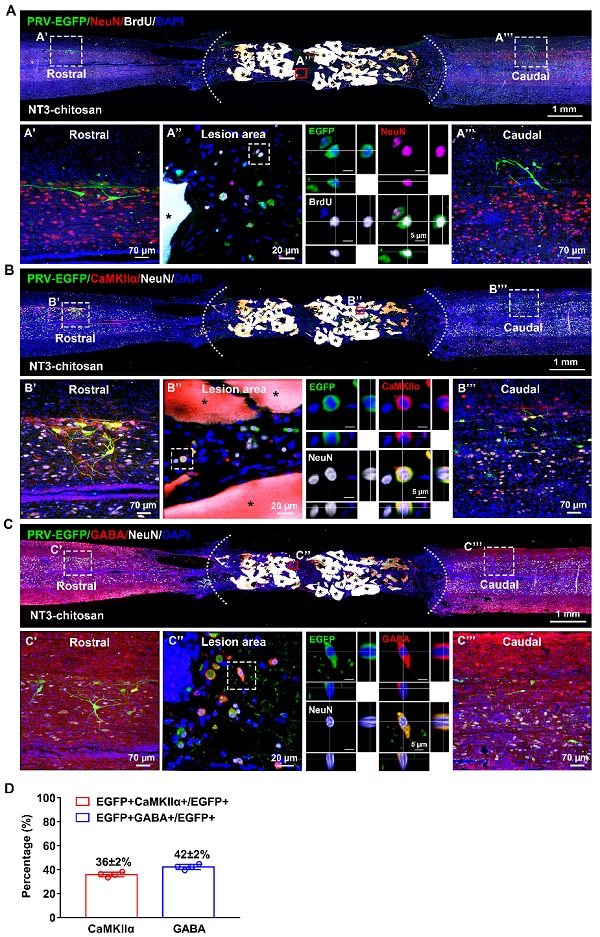
图3. 多重免疫荧光染色证明新生神经元可正确整合到排尿反射神经环路中。
作者简介
本论文的第一作者为北航医学科学与工程学院郝飞;合作者包括北航医学科学与工程学院樊瑜波教授等;北航生物与医学工程学院李晓光教授、同济大学孙毅教授、首都医科大学杨朝阳教授和深圳先进技术研究院徐富强教授为通讯作者,北京航空航天大学为本论文的第一完成单位。
本研究得到了科技部重点研发计划(2017YFC1104001、2017YFC1104002、 2016YFA0100801)、国家自然科学基金(82201542、31730030、81941011、31971279、31900749)和北京市自然科学基金(7214301)等项目的资助,并得到了生物材料与神经再生北京市重点实验室、生物力学与力生物学教育部重点实验室和北京市生物医学工程高精尖创新中心的支持。
全文链接:https://doi.org/10.1016/j.biomaterials.2022.121919